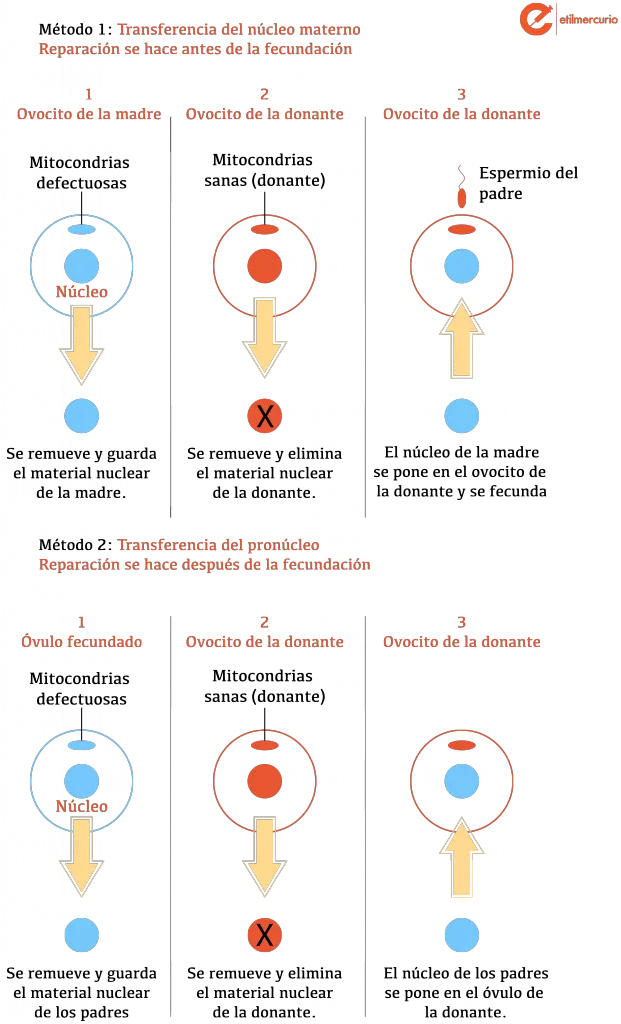En colaboración con Gabriel León.
—Papá ¿puedo salir?
—Pregúntale a tu mamá.
—Mamá ¿puedo salir?
—Pregúntale a tu otra mamá.
Este diálogo —tan común en la adolescencia— tiene un elemento adicional que lo hace sonar algo raro. Después de todo nadie tiene dos mamás biológicas... ¿O sí?
Emma Ott nació en 1997 en Pensilvania y fue la primera persona del mundo que fue concebida a través de una revolucionaria técnica de fertilización in vitro. Sus padres —que no habían podido concebir de manera natural ni mediante los métodos tradicionales de fertilización in vitro— habían decidido someterse a un nuevo tratamiento llamado «transferencia citoplásmica». Los expertos en fertilidad sospechaban que algo andaba mal con las mitocondrias en los ovocitos de algunas mujeres, lo que impedía que lograran concebir. La idea fue que tal vez si le transferían a los ovocitos defectuosos algunas mitocondrias de un ovocito sano podrían lograr una fecundación exitosa. Mediante esta técnica nacieron 17 niños en EEUU, incluyendo Emma. Análisis genéticos realizados a estos niños mostraron que en al menos dos casos se lograba detectar material genético de la donante del citoplasma. Debido a la ausencia de pruebas concluyentes sobre los efectos de esto, la FDA decidió prohibir esta técnica en EEUU el año 2001.
2015, una nueva esperanza.
El pasado 3 de febrero de 2015, la Cámara de los Comunes del Reino Unido (que vendría a ser como la Cámara de Diputados británica) votó a favor de una ley que le permitiría a los científicos británicos continuar con sus investigaciones para la aplicación de lo que era un novedoso tratamiento de fertilidad que podría prevenir algunos casos de enfermedades de origen genético. Se trataba esta vez de una técnica llamada «reemplazo de mitocondrias». Esta técnica podría permitir que mujeres que llevan mutaciones en su ADN mitocondrial —y que causan enfermedades fatales en los hijos— sean capaces de dar a luz a bebés sanos. La aplicación de una técnica como ésta no está exenta de controversias, debido a que se altera la composición genética del embrión, y como el ADN mitocondrial se hereda por vía materna, implica que si la recién nacida es niña, ella heredará inevitablemente las mitocondrias de la donante a sus futuras generaciones en lugar de las mitocondrias de su madre.
Controversial, sin duda, pero creemos que el costo-beneficio lo podría valer.
Como recordarán de sus clases de biología, muchas veces nos dijeron que la mitocondria es «la pila de la célula», lo que dicho en un lenguaje más técnico, implica que éste organelo celular es el responsable de proveer energía a nivel celular (suena importante, ¿no?). Las mitocondrias poseen su propio genoma, compuesto por 37 genes, en comparación al genoma nuclear que tiene más de 20.000 genes identificados. Los genes de la mitocondria se llaman… adivine cómo... ¡Sí, adivinó! ADN mitocondrial, o mitogenoma.
](https://www.etilmercurio.com/em/wp-content/uploads/2016/09/mtdonation-1.png) Ilustración original: Cath Levett, Guardian Graphic. Modificado por Gabriel León
Si la mitocondria no funciona de forma correcta, esto se traduce en una serie de síntomas, lo que hace que las enfermedades de origen mitocondrial sean difíciles de reconocer y por lo tanto difíciles de diagnosticar. Las enfermedades mitocondriales pueden ser graves, incluso hay reportes de bebés que nacen con este tipo de patologías (1) y mueren a los meses de haber nacido. Por otra parte, hay casos de personas que no experimentan síntomas hasta varios años después de nacer (2) (o cuando son «fetos adultos», como diría la Senadora van Rysselberghe).
Para esto, los investigadores han desarrollado una serie de métodos que permiten transferir el material genético de un ovocito (si no está fecundado, no le diga óvulo; es un ovocito) que contiene la mitocondria defectuosa a un ovocito de una donante sana. El resultado de esto es que el embrión resultante luego de la fecundación lleva el ADN nuclear de sus padres y el ADN mitocondrial de una donante. Es decir, estrictamente son un papá, y dos mamás (de las cuales, una mamá aporta/dona solamente las mitocondrias).
A pesar de que hubo controversias al respecto, pues se deberían hacer más estudios para probar la seguridad del método, lo general es que había cierto consenso científico y ético para su aplicación. De hecho, en la revista Nature el año 2014 (3), se publicó un estudio en donde se sugería que mediante la aplicación de esta técnica, era posible producir embriones humanos de aspecto normal, a menos en su estadio de blastocisto (que no tiene nada que ver con Pokémon, si no que es el estado al que llega el embrión luego de aproximadamente 5 días de haber fecundado).
Un poco antes, en 2009, Nature también publicaba algunos ensayos con esta nueva metodología en monos (4), los que resultaron en casos exitosos de reproducción y producción de células madre.
Si lo vemos de la forma más simple posible, y esperando no ofender a nadie, el procedimiento es similar a cambiar una pila defectuosa. Si bien es una analogía muy simple pues la interacción núcleo-mitocondria es mucho más compleja que sólo reemplazar una pieza (cambios menores tanto en el núcleo como en la mitocondria podrían afectar al funcionamiento de esta última), esto podría servir para entender la idea general detrás del método.
Pero bueno, lo cierto es que el 27 de septiembre la ciencia nuevamente nos sorprende con el reporte de un nuevo bebé con «tres padres» (que no es el primero, por cierto, aparte de Emma Ott y los 17 niños que mencionamos al inicio, está Alana Saaranen, quien ya tiene 16 años).
El nuevo anuncio se refiere un bebé que nació hace 5 meses, y el tratamiento fue realizado por un especialista en fertilidad de estados Unidos, Dr. John Zhang (5)... pero en México, donde las leyes para la manipulación de embriones humanos son un poco más laxas.El Dr. Zhang usó una técnica que en español sería algo como «transferencia del eje nuclear» (sprindle nuclear transfer) para poder crear 5 embriones humanos. Este método implica remover el núcleo de la célula desde los ovocitos de la madre e insertarlos al de una donante sana (célula a la cual se le ha removido ya parte del núcleo), dando como resultado ovocitos con mitocondrias saludables de la donante y ADN nuclear de la madre. Estos cinco embriones fueron entonces fecundados con espermatozoides del padre, pero solo uno de estos resultó tener un número normal de cromosomas. Este embrión normal, fue transferido posteriormente a la madre.
El único reporte científico que tenemos al respecto es el resumen de la conclusión de este trabajo, la cual sugiere que:
«los ovocitos humanos reconstituidos mediante SNT (transferencia del eje nuclear) son capaces de producir bebés sanos. El SNT podría ser una novedosa opción para poder minimizar patologías transmitidas por el ADN mitocondrial desde las madres a sus bebés».
Al parecer hay aspectos que aun debemos estudiar respecto a estas técnicas, pero sin duda son un gran avance para prevenir enfermedades genéticas de origen mitocondrial.
Cuando le preguntaron a Arana, la chica de dieciséis años que mencionamos previamente, sobre qué opinaba de tener tres padres, ella respondió:
«Tengo el ADN de una tercera mujer. Pero no la consideraría un tercer padre, sólo tengo algunas de sus mitocondrias (...) Mucha gente dice que tengo los rasgos de mi madre, mis ojos se parecen a los de mi papá… Tengo algunas características de ellos y mi personalidad es la misma también».
Referencias
1.
Koenig MK. Presentation and Diagnosis of Mitochondrial Disorders in Children. Pediatric Neurology. mayo de 2008;38(5):305–13.
2.
Cohen BH. Neuromuscular and Systemic Presentations in Adults: diagnoses beyond MERRF and MELAS. Neurotherapeutics. abril de 2013;10(2):227–42.
3.
Tachibana M, Amato P, Sparman M, Woodward J, Sanchis DM, Ma H, et al. Towards germline gene therapy of inherited mitochondrial diseases. Nature. 24 de octubre de 2012;493(7434):627–31.
4.
Tachibana M, Sparman M, Sritanaudomchai H, Ma H, Clepper L, Woodward J, et al. Mitochondrial gene replacement in primate offspring and embryonic stem cells. Nature. 17 de septiembre de 2009;461(7262):367–72.
5.
J. Zhang, H. Liu, S. Luo, A. Chavez-Badiola, Z. Liu, M. Yang, et al. First live birth using human oocytes reconstitued by spindle nuclear transfer for mitochondrial DNA mutation causing Leigh Syndrome. En Salt Lake City, Utah; 2016 [citado 28 de septiembre de 2016]. Disponible en: [www.west-info.eu]